向硝酸酸化的硝酸银溶液()中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物
①取少量黑色固体,洗涤后, (填操作和现象),证明黑色固体中含有。
②取上层清液,滴加溶液,产生蓝色沉淀,说明溶液中含有 。
(2)针对“溶液呈黄色”,甲认为溶液中有,乙认为铁粉过量时不可能有,乙依据的原理是 (用离子方程式表示)。针对两种观点继续实验:
①取上层清液,滴加溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶液颜色变浅、沉淀量多少与取样时间有关,对比实验记录如下:
|
序号 |
取样时间/ |
现象 |
|
|
|
产生大量白色沉淀;溶液呈红色 |
|
|
|
产生白色沉淀;较时量小;溶液红色 |
|
|
|
产生白色沉淀;较时量小;溶液红色 |
②对产生的原因作出如下假设:
假设:可能是铁粉表面有氧化层,能产生;
假设:空气中存在,由于 (用离子方程式表示),可产生;
假设:酸性溶液中具有氧化性,可产生;
假设:根据 现象,判断溶液中存在,可产生。
③下列实验Ⅰ可证实假设、、不是产生的主要原因.实验Ⅱ可证实假设成立。
实验Ⅰ:向硝酸酸化的 溶液()中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加溶液,时溶液呈浅红色,后溶液几乎无色。
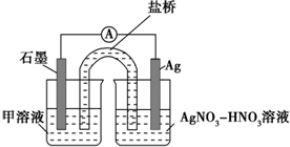
实验Ⅱ:装置如图.其中甲溶液是 ,操作及现象是 。
(3)根据实验现象,结合方程式推测实验中浓度变化的原因: 。
水中溶氧量()是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位,我国《地表水环境质量标准》规定,生活饮用水源的不能低于。某化学小组同学设计了下列装置(夹持装置略),测定某河水的。
、测定原理:
碱性条件下,将氧化为:①
酸性条件下,将氧化为:②(未配平),用标准溶液滴定生成的:③
、测定步骤
.安装装置,检验气密性,充排尽空气后,停止充。
.向烧瓶中加入水样。
.向烧瓶中依次迅速加入无氧溶液(过量)、碱性无氧溶液(过量),开启搅拌器,至反应①完全。
.搅拌并向烧瓶中加入硫酸无氧溶液至反应②完全,溶液为中性或弱酸性。
.从烧瓶中取出溶液,以淀粉作指示剂,用溶液进行滴定,记录数据。
.……
.处理数据(忽略氧气从水样中的逸出量和加入试剂后水样体积的变化)。
回答下列问题:
(1)配置以上无氧溶液时,除去所用溶剂水中氧的简单操作为_____。
(2)在橡胶塞处加入水样及有关试剂应选择的仪器为_____。
①滴定管②注射器③量筒
(3)搅拌的作用是_____。
(4)配平反应②的方程式,其化学计量数依次为_____。
(5)步骤为_____。
(6)步骤中达到滴定终点的标志为_____。若某次滴定消耗溶液,水样的_____(保留一位小数)。作为饮用水源,此次测得是否达标:_____(填是或否)
(7)步骤中加入硫酸溶液反应后,若溶液过低,滴定时会产生明显的误差,写出产生此误差的原因(用离子方程式表示,至少写出个)_____。
和会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题。
Ⅰ.的除去
方法:生物脱的原理为:
(1)硫杆菌存在时,被氧化的速率是无菌时的倍,该菌的作用是 。
(2)由图和图判断使用硫杆菌的最佳条件为 。若反应温度过高,反应速率下降,其原因是 。
方法:在一定条件下,用氧化
(3)随着参加反应的变化,氧化产物不同。当时,氧化产物的分子式为 。
Ⅱ.的除去
方法(双碱法):用吸收,并用使再生
(4)写出过程①的离子方程式: ;在水中存在如下转化:
从平衡移动的角度,简述过程②再生的原理 。
方法:用氨水除去
(5)已知,的,的。若氨水的浓度为,溶液中的 。将通入该氨水中,当降至时,溶液中的 。
丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷脱氢制丁烯的热化学方程式如下:
①
已知:②
③
反应①的为 。图是反应①平衡转化率与反应温度及压强的关系图, (填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是 (填标号)。
升高温度 降低温度 增大压强 降低压强
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图()为丁烯产率与进料气中(氢气)(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是 。
(3)图()为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在之前随温度升高而增大的原因可能是 、 ;之后,丁烯产率快速降低的主要原因可能是
。
东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_____,能级上的未成对的电子数为_____。
(2)硫酸镍溶于氨水形成蓝色溶液。
①中阴离子的立体构型是_____。
②在中与之间形成的化学键称为_____,提供孤电子对的成键原子是_____。
③氨的沸点_____(“高于”或“低于”)膦(),原因是_____;氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_____。
(3)单质铜及镍都是由_____键形成的晶体:元素同与镍的第二电离能分别为:,,的原因是_____。
(4)某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为,晶胞参数_____。