元素铬()在溶液中主要以(蓝紫色)、(绿色)、(橙红色)、(黄色)等形式存在,为难溶于水的灰蓝色固体,回答下列问题:
(1)与的化学性质相似。在溶液中逐滴加入溶液直至过量,可观察到的现象是_____。
(2)和在溶液中可相互转化。室温下,初始浓度为的溶液中随的变化如图所示。
①用离子方程式表示溶液中的转化反应_____。
②由图可知,溶液酸性增大,的平衡转化率_____(填“增大”“减小”或“不变”)。根点数据,计算出该转化反应的平衡常数为_____。
③升高温度,溶液中的平衡转化率减小,则该反应的_____(填“大于”“小于”或“等于”)。
(3)在化学分析中采用为指示剂,以标准溶液滴定溶液中,利用与生成砖红色沉淀,指示到达滴定终点。当溶液中恰好沉淀完全(浓度等于)时,溶液中为_____,此时溶液中等于_____。(已知、的分别为和)。
(4)价铬的化合物毒性较大,常用将废液中的还原成,该反应的离子方程式为_____。
(图中虚线表示氢键)
下列说法不正确的是( )
凯氏定氨法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。
已知:;。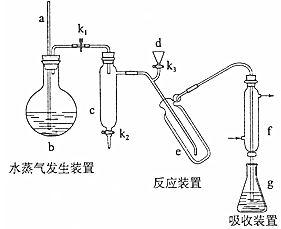
回答下列问题:
(1)的作用是 。
(2)中放入少量碎瓷片的目的是 。的名称是 。
(3)清洗仪器:中加蒸馏水:打开,关闭、,加热,蒸气充满管路:停止加热,关闭,中蒸馏水倒吸进入,原因是 ;打开放掉水,重复操作次。
(4)仪器清洗后,中加入硼酸()和指示剂,铵盐试样由注入,随后注入氢氧化钠溶液,用蒸馏水冲洗,关闭,中保留少量水,打开,加热,使水蒸气进入。
①中保留少量水的目的是 。
②中主要反应的离子方程式为 ,采用中空双层玻璃瓶的作用是 。
(5)取某甘氨酸()样品克进行测定,滴定中吸收液时消耗浓度为的盐酸,则样品中氮的质量分数为 ,样品的纯度 。
锗()是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态原子的核外电子排布式为_____,有_____个未成对电子。
(2)与是同族元素,原子之间可以形成双键、叁键,但原子之间难以形成双键或叁键。从原子结构角度分析,原因是_____。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____。
| 熔点 | |||
| 沸点 | 约 |
(4)光催化还原制备反应中,带状纳米是该反应的良好催化剂。、、电负性由大至小的顺序是_____。
(5)单晶具有金刚石型结构,其中原子的杂化方式为_____,微粒之间存在的作用力是_____。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为单晶的晶胞,其中原子坐标参数为,为;为。则原子的坐标参数为_____。
②晶胞参数,描述晶胞的大小和形状,已知单晶的晶胞参数,其密度为_____(列出计算式即可)。
(1)的结构简式为 。的化学名称是 。
(2)③的反应试剂和反应条件分别是 ,该反应的类型是 。
(3)⑤的反应方程式为 。吡啶是一种有机碱,其作用是 。
(4)的分子式为 。
(5)是的同分异构体,其苯环上的取代基与的相同但位置不同,则可能的结构有 种。
(6)甲氧基乙酰苯胺()是重要的精细化工中间体,写出由苯甲醚()制备甲氧基乙酰苯胺的合成路线 (其他试剂任选)。
|
目的 |
操作 | |
| 取盐酸 |
在酸式滴定管中装入盐酸,调整初始 读数为后,将剩余盐酸放入锥形瓶 | |
| 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 | |
| 测定醋酸钠溶液 | 用玻璃棒蘸取溶液,点在湿润的试纸上 | |
|
配制浓度为的 |
称取固体,放入容量 瓶中,加水溶解并稀释至刻度 |
已知:①
②
回答下列问题:
(1)化学式名称为 。
(2)由生成和生成的反应类型分别为 、 。
(3)的结构简式为 。
(4)为甲苯的同分异构体,由生成H的化学方程式为 。
(5)芳香化合物是的同分异构体,能与饱和碳酸氢钠溶液反应放出,其核磁共振氢谱显示有种不同化学环境的氢,峰面积比为,写出种符合要求的的结构简式 。
(6)写出用环戊烷和丁炔为原料制备化合物的合成路线 (其他试剂任选)。
水中溶氧量()是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位,我国《地表水环境质量标准》规定,生活饮用水源的不能低于。某化学小组同学设计了下列装置(夹持装置略),测定某河水的。
、测定原理:
碱性条件下,将氧化为:①
酸性条件下,将氧化为:②(未配平),用标准溶液滴定生成的:③
、测定步骤
.安装装置,检验气密性,充排尽空气后,停止充。
.向烧瓶中加入水样。
.向烧瓶中依次迅速加入无氧溶液(过量)、碱性无氧溶液(过量),开启搅拌器,至反应①完全。
.搅拌并向烧瓶中加入硫酸无氧溶液至反应②完全,溶液为中性或弱酸性。
.从烧瓶中取出溶液,以淀粉作指示剂,用溶液进行滴定,记录数据。
.……
.处理数据(忽略氧气从水样中的逸出量和加入试剂后水样体积的变化)。
回答下列问题:
(1)配置以上无氧溶液时,除去所用溶剂水中氧的简单操作为_____。
(2)在橡胶塞处加入水样及有关试剂应选择的仪器为_____。
①滴定管②注射器③量筒
(3)搅拌的作用是_____。
(4)配平反应②的方程式,其化学计量数依次为_____。
(5)步骤为_____。
(6)步骤中达到滴定终点的标志为_____。若某次滴定消耗溶液,水样的_____(保留一位小数)。作为饮用水源,此次测得是否达标:_____(填是或否)
(7)步骤中加入硫酸溶液反应后,若溶液过低,滴定时会产生明显的误差,写出产生此误差的原因(用离子方程式表示,至少写出个)_____。
己烷雌酚的一种合成路线如下:
下列叙述正确的是 ( )